Hóa học 11 KNTT Bài 6: Một số hợp chất của nitrogen với oxygen
1.1. Các oxide của nitrogen
a. Công thức, tên gọi
Oxide của nitrogen được kí hiệu chung là NOx, một loại hợp chất điển hình gây ô nhiễm không khí. Hợp chất NOx có trong không khí là NO2, NO, N2O4, N2O
|
Oxide |
Tên gọi |
|
N2O |
Dinitrogen oxide |
|
NO |
Nitrogen monoxide |
|
NO2 |
Nitrogen dioxide |
|
N2O4 |
Dinitrogen tetroxide |
b. Nguồn gốc phát sinh NOx trong không khí
− Bên cạnh nguồn gốc tự nhiên như:
+ Núi lửa phun trào
+ Cháy rừng
+ Mưa dông kèm theo sấm sét
+ Sự phân huỷ các hợp chất hữu cơ thì sự phát sinh NOx chủ yếu là do hoạt động của con người.
− Các nguồn gây phát thải NOx nhân tạo từ hoạt động giao thông vận tải, sản xuất công nghiệp, nông nghiệp, nhà máy nhiệt điện và trong đời sống.
Bảng 6.1. Nguyên nhân hình thành NOx trong không khí
- NOx là một trong các nguyên nhân gây mưa acid, sương mù quang hoá, hiệu ứng nhà kính, thủng tầng ozone và hiện tượng phú dưỡng, làm ô nhiễm môi trường.
(1) Sinh khối là một thuật ngữ dùng để mô tả các vật chất hữu cơ có nguồn gốc từ sinh vật sống.
(2) Gốc tự do là nguyên tử/nhóm nguyên tử có electron tự do, chưa tạo thành cặp electron.
c. Mưa acid
− Nước mưa thông thường có pH khoảng 5,6 chủ yếu do có carbon dioxide hoà tan tạo môi trường acid yếu.
− Khi nước mưa có pH nhỏ hơn 5,6 thì gọi là hiện tượng mưa acid.
− Tác nhân chính gây mưa acid là SO2 và NOx phát thải chủ yếu do các hoạt động công nghiệp, nhiệt điện, giao thông, khai thác và chế biến dầu mỏ,....
− Với sự xúc tác của các ion kim loại trong khói bụi, khí SO2 và NOx bị oxi hoá bởi oxygen, ozone, hydrogen peroxide, gốc tự do,... rồi hoà tan vào nước, tạo thành sulfuric acid và nitric acid.
Ví dụ:
SO2 + 2H2O \(\xrightarrow{{{xúc\ tác}}}\) 2H2SO4
4NO2 + O2 + H2O \(\xrightarrow{{{xúc\ tác}}}\) 4HNO3
− Các giọt acid li ti tạo thành theo mưa rơi xuống bề mặt Trái Đất.
− Mưa acid gây tác động xấu đối với môi trường, con người và sinh vật, rõ rệt nhất khi nước mưa có giá trị pH dưới 4,5. Mưa acid, ảnh hưởng đến sinh vật, ăn mòn các công trình xây dựng, kiến trúc bằng đá và kim loại,...
1.2. Nitric acid
a. Cấu tạo
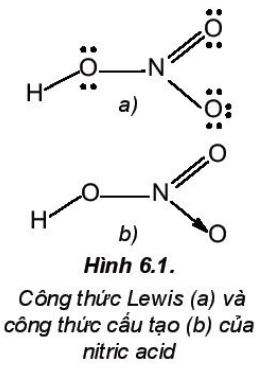
− Nitric acid (HNO3) có công thức Lewis và công thức cũng trúc Lama và công trực cấu tạo như Hình 6.1.
− Đặc điểm cấu tạo của phân tử nitric acid:
+ Nguyên tử N có số oxi hoá +5, là số oxi hoá cao nhất của nitrogen.
+ Liên kết O-H phân cực mạnh về phía nguyên tử oxygen.
+ Liên kết N → O là liên kết cho nhận.
b. Tính chất vật lí
Nitric acid tinh khiết là chất lỏng, không màu, có khối lượng riêng D = 1,53 g/mL. Nitric acid nóng chảy ở – 42°C và sôi ở 83°C. Nitric acid bốc khói mạnh trong không khí ẩm và tan vô hạn trong nước.
c. Tính chất hoá học
Tính acid
− Nitric acid có khả năng cho proton, thể hiện tính chất của một acid Bronsted-Lowry.
− Trong công nghiệp, nitric acid được sử dụng để sản xuất phân bón giàu dinh dưỡng như ammonium nitrate, calcium nitrate.
NH3 + HNO3 \(\to\) NH4NO3
CaCO3 + 2HNO3 \(\to\) Ca(NO3)2+CO2+H2O
− Ammonium nitrate cung cấp nguyên tố nitrogen ở cả dạng ammonium và cả dạng nitrate.
Tính oxi hoá
Phân tử nitric acid chứa nguyên tử nitrogen có số oxi hoá cao nhất (+5) nên nitric acid có khả năng nhận electron, thể hiện tính oxi hoá mạnh.
1.3. Hiện tượng phú dưỡng
− Nguyên nhân của hiện tượng phú dưỡng là do sự dư thừa dinh dưỡng đã cung cấp nguồn thức ăn dồi dào cho sinh vật phù du phát triển rất mạnh.
− Thông thường, khi hàm lượng nitrogen trong nước (bao gồm ion nitrate, nitrite, ammonium) đạt 300 \(\text{ }\!\!\mu\!\!\text{ }\)g/L và hàm lượng phosphorus (các dạng ion phosphate) đạt 20 \(\text{ }\!\!\mu\!\!\text{ }\)g/L sẽ gây ra hiện tượng phú dưỡng.