Hóa học 11 KNTT Bài 4: Nitrogen
1.1. Trạng thái tự nhiên
− Trong khí quyển Trái Đất, nitrogen là nguyên tố phổ biến nhất, chiếm 75,5% khối lượng (hoặc 78,1% thể tích) và tập trung chủ yếu ở tầng đối lưu.
− Trong vỏ Trái Đất, nguyên tố nitrogen tồn tại tập trung ở một số mỏ khoáng dưới dạng sodium nitrate (thường gọi là diêm tiêu Chile).
− Nguyên tố nitrogen có trong tất cả cơ thể động vật và thực vật, là thành phần cấu tạo nên nucleic acid, protein,… Trong cơ thề người, nitrogen chiếm khoảng 3% khối lượng, đứng thứ tư sau oxygen, carbon và hydrogen.
− Nguyên tố nitrogen tồn tại trong tự nhiên với hai đồng vị bền là 14N (99,63%) và 15N (0,37%).
1.2. Cấu tạo nguyên tử, phân tử
a. Cấu tạo nguyên tử
| Nguyên tố nitrogen ở ô số 7, nhóm VA, chu kì 2 trong bảng tuần hoàn. |
− Nguyên tử nitrogen có độ âm điện lớn (3,04).
− Nitrogen là phi kim điển hình.
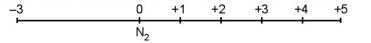
− Nitrogen tạo ra nhiều hợp chất với các số oxi hoá khác nhau từ –3 đến +5.
− Các số oxi hoá thường gặp của nitrogen được biểu diễn ở trục số oxi hoá dưới đây.
b. Cấu tạo phân tử
| Phân tử nitrogen gồm hai nguyên tử, liên kết với nhau bằng liên kết ba (1 liên kết sigma và 2 liên kết pi). Phân tử nitrogen có năng lượng liên kết lớn (945 kJ/mol) và không có cực. |
1.3. Tính chất vật lí
Ở điều kiện thường, nitrogen là chất khí, không màu, không mùi, không vị, khó hoá lỏng (hoá lỏng ở –196 °C), tan rất ít trong nước ( 1 lít nước hoà tan được 0,012 lít khí nitrogen). Khí nitrogen không duy trì sự cháy và sự hô hấp.
1.4. Tính chất hoá học
a. Tác dụng với hdrogen
Ở nhiệt độ cao, áp suất cao và có xúc tác, nitrogen hoá hợp trực tiếp với hydrogen, tạo thành ammonia.
N2(g) + 3H2(g) \(\rightleftharpoons\) 2NH3(g)
b. Tác dụng với oxygen
Ở nhiệt độ cao trên 3000 °C hoặc có tia lửa điện, nitrogen kết hợp với oxygen, tạo ra nitrogen monoxide (NO) với hiệu suất rất thấp.
N2(g)+O2(g)\(\rightleftharpoons\) 2NO(g) \({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\) = 180,6 kJ
Quá trình tạo và cung cấp đạm nitrate cho đất từ nước mưa được biểu diễn theo sơ đồ:
\({{\text{N}}_{\text{2}}}\xrightarrow{\text{+}\,{{\text{O}}_{\text{2}}}}\text{NO}\xrightarrow{\text{+}\,{{\text{O}}_{\text{2}}}\text{+}\,{{\text{H}}_{\text{2}}}\text{O}}\text{HN}{{\text{O}}_{\text{3}}}\xrightarrow{+\,{{\text{O}}_{2}}}{{\text{H}}^{\text{+}}}\text{+}\,\text{N}{{\text{O}}_{\text{3}}}^{\text{-}}\)
1.5. Ứng dụng
− Tác nhân làm lạnh
− Tổng hợp amonia
− Tạo khí quyển trơ
− Bảo quản thực phẩm