Hóa học 11 KNTT Bài 1: Khái niệm về cân bằng hoá học
1.1. Phản ứng một chiều và phản ứng thuận nghịch
a. Phản ứng một chiều
− Xét phản ứng đốt cháy khí methane trong khí oxygen:
CH4 + 2O2 \(\xrightarrow{{{t}^{o}}}\) CO2 + 2H2O
− Khi đốt cháy khí methane, thu được sản phẩm là khi carbon dioxide và hơi nước. Trong điều kiện này, các chất sản phẩm không phản ứng được với nhau để tạo thành chất đầu. Phản ứng như trên được gọi là phản ứng một chiều.
− Phương trình hoá học của phản ứng một chiều được biểu diễn bằng một mũi tên chỉ chiều phản ứng (\(\to\)).
Ví dụ: NaOH + HCl \(\to\) NaCl + H2O.
b. Phản ứng thuận nghịch
− Xét phản ứng của khí hydrogen và iodine trong bình kín ở nhiệt độ 4450C, có hai phản ứng xảy ra đồng thời:
H2(g) + I2(g) \(\to\) 2HI(g)
2HI(g) \(\to\) H2(g) + I2(g)
− Ở thí nghiệm trên, khí H2 tác dụng với I2 tạo thành HI, đồng thời HI lại phân huỷ tạo thành I2 và H2 nên dù thời gian kéo dài bao lâu, phản ứng vẫn không thể xảy ra hoàn toàn. Phản ứng giữa H2 và I2, trong điều kiện trên được gọi là phản ứng thuận nghịch và được biểu diễn bằng phương trình hoá học:
H2(g) + I2(g) \(\rightleftharpoons\) 2HI(g)
|
− Phản ứng thuận nghịch là phản ứng xảy ra theo hai chiều ngược nhau trong cùng điều kiện. − Phương trình hoá học của phản ứng thuận nghịch được biểu diễn bằng hai nửa mũi tên ngược chiều nhau ( \(\rightleftharpoons\) ). Chiều từ trái sang phải là chiều phản ứng thuận, chiều từ phải sang trái là chiều phản ứng nghịch. |
1.2. Cân bằng hoá học
a. Trạng thái cân bằng
− Xét phản ứng thuận nghịch:
H2(g) + I2(g) \(\rightleftharpoons\) 2HI(g)
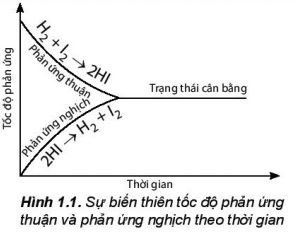
− Lúc đầu phản ứng thuận có tốc độ lớn hơn phản ứng nghịch và ưu tiên tạo ra hydrogen iodide. Theo thời gian, tốc độ phản ứng thuận giảm dần, tốc độ phản ứng nghịch tăng dần đến khi tốc độ hai phản ứng bằng nhau (Hình 1.1). Tại thời điểm này, số mol của các chất hydrogen, iodine, hydrogen iodide không thay đổi nữa. Đây là thời điểm phản ứng thuận nghịch đạt tới trạng thái cân bằng.
|
− Trạng thái cân bằng của phản ứng thuận nghịch là trạng thái tại đó tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch. − Cân bằng hoá học là một cân bằng động, các chất tham gia phản ứng liên tục phản ứng với nhau để tạo thành sản phẩm và các chất sản phẩm cũng liên tục phản ứng với nhau để tạo thành các chất đầu nhưng với tốc độ bằng nhau nên ở trạng thái cần bằng, nồng độ các chất không thay đổi. |
b. Hằng số cân bằng
Biểu thức của hằng số cân bằng
- Xét phản ứng thuận nghịch:
H2(g) + I2(g) \(\rightleftharpoons\) 2HI(g)
+ \({K_C} = \frac{{{\rm{ }}{{[{\rm{ }}HI]}^2}}}{{{\rm{ }}[{\rm{ }}{H_2}{\rm{ }}]{\rm{ }}[{\rm{ }}{I_2}{\rm{ }}]{\rm{ }}}}\) được gọi là biểu thức hằng số cân bằng của phản ứng thuận nghịch.
+ Dấu ngoặc vuông [A] biểu thị nồng độ chất A ở trạng thái cân bằng.
- Xét phản ứng thuận nghịch tổng quát:
aA + bB \(\rightleftharpoons\) cC + dD
|
Ở trạng thái cân bằng, hằng số cân bằng (Kc) của phản ứng được xác định theo biểu thức: \({{K}_{C}}=\frac{\text{ }{{[\text{ C}]} ^{c}}\ {{\text{ }\!\![\!\!\text{ }\ D\ \text{ }\!\!]\!\!\text{ }}\ ^{d}}}{\text{ }{{[\text{ }A\text{ }]}^{a}}\text{ }[\text{ }B\text{ }]{{}^{b}}\text{ }}\) |
+ Trong đó: [A], [B], [C], [D] là nồng độ mol của các chất A, B, C, D ở trạng thái cân bằng; a, b, c, d là hệ số tỉ lượng của các chất trong phương trình hoá học của phản ứng.
+ Thực nghiệm cho thấy: hằng số cân bằng Kc của một phản ứng thuận nghịch chỉ phụ thuộc nhiệt độ và bản chất của phản ứng.
+ Đối với các phản ứng có chất rắn tham gia, không biểu diễn nồng độ của chất rắn trong biểu thức hằng số cân bằng.
Ví dụ: C(s) + CO2(g) \(\rightleftharpoons\) 2CO(g) \({{K}_{C}}=\frac{\text{ }{{[CO]}^{2}}}{\text{ }[\text{ C}{{\text{O}}_{2}}]\text{ }}\)
Ý nghĩa của hằng số cân bằng
- Hằng số cân bằng Kc phụ thuộc vào bản chất của phản ứng và nhiệt độ.
- Biểu thức xác định hằng số cân bằng \({{K}_{C}}=\frac{\text{ }{{[\text{ C}]} ^{c}}\ {{\text{ }\!\![\!\!\text{ }\ D\ \text{ }\!\!]\!\!\text{ }}\ ^{d}}}{\text{ }{{[\text{ }A\text{ }]}^{a}}\text{ }[\text{ }B\text{ }]{{}^{b}}\text{ }}\), cho thấy: Kc càng lớn thì phản ứng thuận càng chiếm ưu thế hơn và ngược lại, Kc càng nhỏ thì phản ứng nghịch càng chiếm chiếm ưu thế hơn.
1.3. Các yếu tố ảnh hưởng đến sự chuyển dịch cân bằng hoá học
a. Ảnh hưởng của nhiệt độ
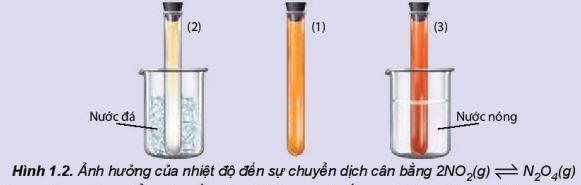
Xét thí nghiệm 1: 2NO2(g) \(\rightleftharpoons\) N2O4(g) \({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\) < 0
Chuẩn bị: 3 ống nghiệm chứa khí NO2 (màu nâu đỏ), nút kín có màu giống nhau, cốc nước đá, cốc nước nóng.
Tiến hành:
– Ống nghiệm (1) để so sánh.
- Ngâm ống nghiệm (2) vào cốc nước đá trong khoảng 1 – 2 phút.
– Ngâm ống nghiệm (3) vào cốc nước nóng trong khoảng 1 – 2 phút.
Lưu ý: NO2 là một khí độc nên phải đậy kín nút.
|
Khi tăng nhiệt độ, cân bằng chuyển dịch theo chiều làm giảm nhiệt độ, tức là chiều phản ứng thu nhiệt ( \({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\) > 0), nghĩa là chiều làm giảm tác động của việc tăng nhiệt độ và ngược lại. |
b. Ảnh hưởng của nồng độ
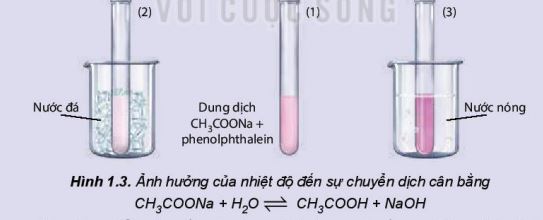
Xét thí nghiệm 2: CH3COONa + H2O \(\rightleftharpoons\) CH3COOH + NaOH \({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\) > 0
Chuẩn bị: dung dịch CH3COONa 0,5 M, phenophtalein; cốc nước nóng, cốc nước đá, 3 ống nghiệm.
Tiến hành:
- Cho khoảng 10 mL dung dịch CH3COONa 0,5 M vào cốc thuỷ tinh, thêm 1 – 2 giọt phenolphthalein, khuấy đều.
– Chia dung dịch thu được vào 3 ống nghiệm. Ống nghiệm (1) để so sánh, ống nghiệm (2) ngâm vào cốc nước đá, ống nghiệm (3) ngâm vào cốc nước nóng.
|
Khi tăng nồng độ một chất trong phản ứng thì cân bằng hoá học bị phá vỡ và chuyển dịch theo chiều làm giảm nồng dộ của chất đó và ngược lại. |
c. Ảnh hưởng của áp suất
Xét thí nghiệm 3: 2NO2(g) \(\rightleftharpoons\) N2O4(g) \({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\) < 0
Lấy một ống xi-lanh đựng khí NO2. Đẩy pít-tông xuống để làm giảm thể tích và làm tăng áp suất trong ống. Lúc này, màu của khí trong xi-lanh đậm hơn. Sau một thời gian, khí trong ống lại nhạt màu hơn (Hình 1.5). Như vậy, khi tăng áp suất, cân bằng trên chuyển dịch theo chiều làm giảm số mol khí trong xi-lanh.
|
Khi tăng áp suất chung của hệ thì cân bằng sẽ chuyển dịch theo chiều làm giảm áp suất, tức là chiều làm giảm số mol khí và ngược lại |
− Đối với phản ứng thuận nghịch có tổng hệ số tỉ lượng của các chất khí ở hai vế phương trình hoá học bằng nhau thì trạng thái cân bằng của hệ không bị chuyển dịch khi thay đổi áp suất chung của hệ.
− Đối với các phản ứng thuận nghịch xảy ra với tốc độ chậm thì chất xúc tác giúp hệ phản ứng nhanh đạt tới trạng thái cân bằng. Chất xúc tác làm tăng tốc độ phản ứng thuận và phản ứng nghịch với số lần bằng nhau nên không làm chuyển dịch cân bằng.
d. Nguyên lí chuyển dịch cân bằng Le Chatelier
− Qua việc nghiên cứu các yếu tố ảnh hưởng đến cân bằng, nhà hoá học người Pháp Le Chatelier (Lơ Sa-tơ-li-ê) đã đưa ra một nguyên lí mang tên ông như sau:
|
Một phản ứng thuận nghịch đang ở trạng thái cân bằng, khi chịu một tác động bên ngoài làm thay đổi nồng độ, nhiệt độ, áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó. |
− Nguyên lí chuyển dịch cân bằng Le Chatelier có ý nghĩa rất lớn khi được vận dụng vào kĩ thuật công nghiệp hoá học. Người ta có thể thay đổi các điều kiện để chuyển dịch cân bằng theo chiều mong muốn, làm tăng hiệu suất của phản ứng.