2.1. Khái niệm, phân loại và danh pháp Amin
a. Khái niệm, phân loại
– Khi thay thế nguyên tử H trong phân tử NH3 bằng gốc hidrocacbon ta thu được Amin.
– Amin thường có đồng phân về mạch Cacbon, về vị trí nhóm chức và về bậc Amin.
– Phân loại:
Theo gốc hidrocacbon:
+ Amin mạch hở: CH3NH2 (Metylamin), C2H5NH2 (Etylamin),…
+ Amin thơm: C6H5NH2 (Phenylamin),…
Theo bậc của Amin ( Bậc amin thường được tính bằng số gốc hidrocacbon liên kết với nguyên tử N):
+ Amin bậc I: CH3NH2, C2H5NH2, …
+ Amin bậc II: CH3-NH-CH3
+ Amin bậc III: CH3N(CH3)CH3
b. Danh pháp
– Danh pháp gốc – chức: tên gốc Hidrocacbon + amin
– Ví dụ: CH3-NH-CH3 (Đimetylamin); (CH3)3N (Trimetylamin); …
2.2. Tính chất vật lí của Amin
– Metyl-, đimetyl-, trimetyl- và etylamin là những chất khí mùi khai, độc, dễ tan trong nước. Các amin đồng đẳng cao hơn là chất lỏng hoặc rắn.
– Anilin là chất lỏng, rất độc, nhiệt độ sôi 184oC, ít tan trong nước, tan trong ancol…
– Các Amin đều độc.
2.3. Cấu tạo phân tử và tính chất hóa học của Amin
a. Cấu tạo phân tử
– Amin có tính bazơ và dễ bị oxi hóa tương tự NH3.
– Amin còn có tính chất của gốc hidrocacbon.
b. Tính chất hóa học
– Tính bazơ: Dung dịch Metylamin hoặc Propylamin làm màu quỳ chuyển xanh, còn Anilin thì quỳ tím không đổi màu.
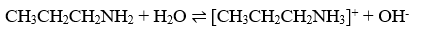
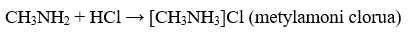
– Tính bazơ của amin phụ thuộc mật độ e trên nguyên tử N: mật độ e lớn, tính bazơ mạnh
+ Gốc HC đẩy e làm tăng tính bazơ
+ Gốc hút e làm giảm tính bazơ
+ Amin béo > NH3 > amin thơm
+ Amin béo bậc II > amin béo bậc I
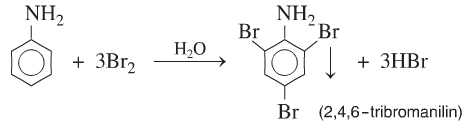
+ Phản ứng thế ở nhân thơm của Anilin: