1.1. Năng lượng và sự chuyển hóa năng lượng trong tế bào
a. Các dạng năng lượng trong tế bào
– Năng lượng trong tế bào tồn tại chủ yếu dưới các dạng như năng lượng hoá học, năng lượng cơ học, năng lượng điện, năng lượng nhiệt. Trong đó, năng lượng hoa học là năng lượng dự trữ trong các liên kết hoá học. Năng lượng cơ học, năng lượng điện, năng lượng nhiệt (Q) là các dạng năng lượng liên quan đến sự chuyển động của các phần tử vật chất.
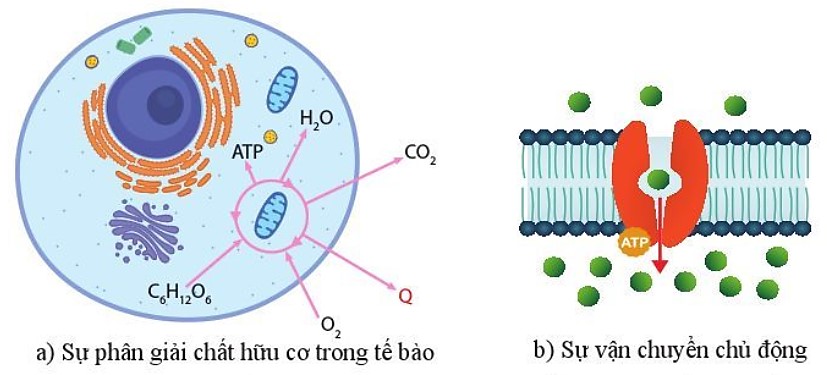
Hình 10.2. Sự chuyển hoá năng lượng trong một số hoạt động sống của tế bào
b. Sự chuyển hoá năng lượng trong tế bào
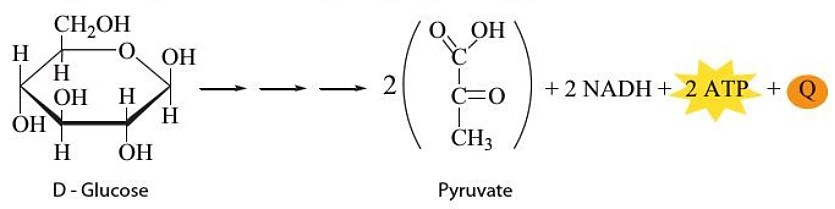
Hình 10.3. Quá trình phân giải glucose
Theo Định luật bảo toàn năng lượng, năng lượng không tự nhiên được sinh ra và cũng không tự nhiên mất đi mà chỉ chuyển từ dạng này sang dạng khác. Dạng năng lượng chủ yếu trong tế bảo là năng lượng hoa học. Toàn bộ các phản ứng (sự trao đổi vật chất) đều xảy ra đồng thời với sự chuyển hoa năng lượng. Do vậy, sự chuyển hóa năng lượng trong tế bào có thể hiểu là quá trình biến đổi năng lượng từ dạng này sang dạng khác, từ năng lượng trong hợp chất này thành năng lượng trong hợp chất khác. Tế bào sử dụng năng lượng thực hiện các hoạt động sống đảm bảo sự tồn tại, sinh trưởng, phát triển và sinh sản
| Trong tế bào, năng lượng tồn tại ở nhiều dạng khác nhau nhưng dạng chủ yếu là năng lượng hoá học. Sự chuyển hoá năng lượng trong tế bào là quá trình biến đổi năng lượng tử dạng này sang dạng khác, từ năng lượng trong hợp chất này thành năng lượng trong hợp chất khác. |
c. ATP – “đồng tiền” năng lượng
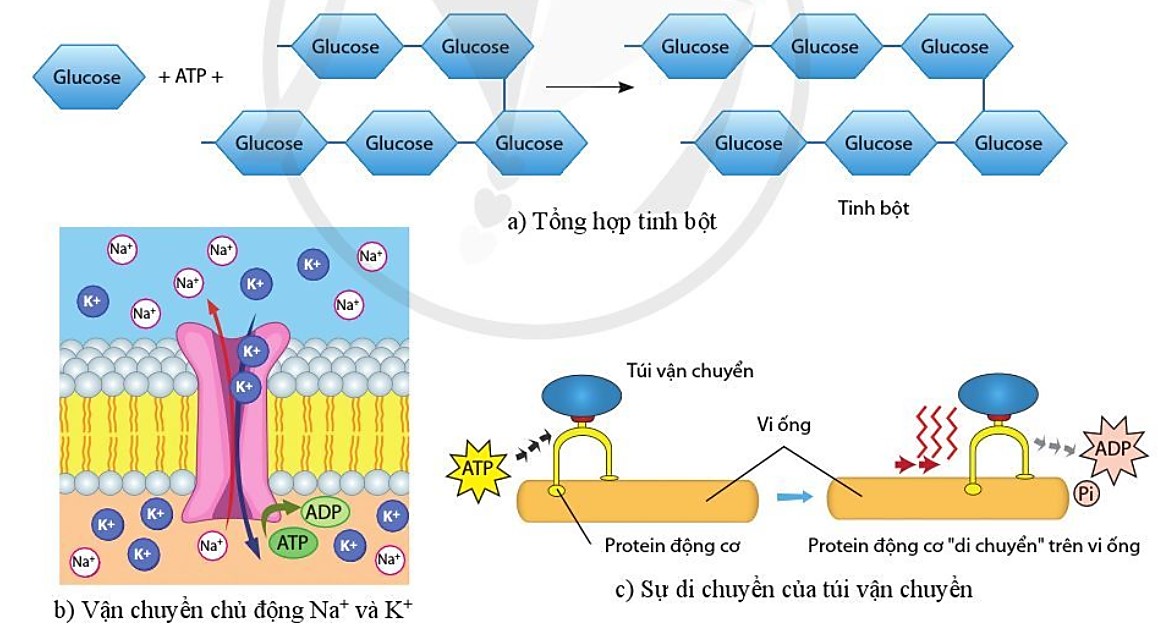
Hình 10.4. Một số hoạt động cần năng lượng của tế bào
– Tinh bột, glycogen và triglyceride là các phân tử dự trữ năng lượng nhưng sự phân giải các phân tử này và các đơn phản của chúng không thể cung cấp năng lượng trực tiếp cho các hoạt động sống của tế bảo mả gián tiếp thông qua ATP
– Phân tử ATP có 3 gốc phosphate. Khi liên kết giữa hai gốc phosphate của ATP bị phá vỡ năng lượng được chuyển hoa trực tiếp cho các hoạt động cần năng lượng của tế bào. Sự phân giải các hợp chất dự trữ năng lượng cung cấp năng lượng cho sự hình thành liên kết giữa các gốc phosphate trong phân tử ATP Vi vậy ATP đóng vai trò là “đồng tiền” năng lượng của tế bào.
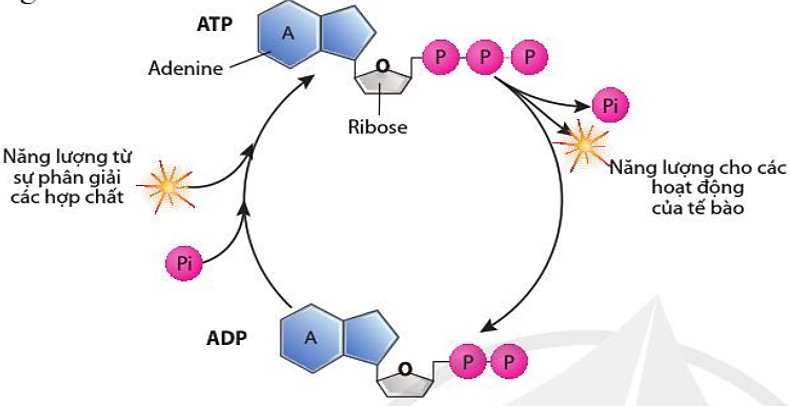
Hình 10.5. Chu trình phân giải và tổng hợp ATP
| ATP là nucleotide có ba góc phosphate, là “đồng tiền” năng lượng của tế bào. Khi ATP bị phân giải, năng lượng được chuyển hoá cho các hoạt động của tế bào. ATP được tổng hợp từ sự chuyển hoá năng lượng trong quá trình phân giải các hợp chất. |
1.2. Enzyme
a. Khái niệm và vai trò của enzyme
– Thuật ngữ enzyme được đề xuất vào cuối thế kỉ XIX để chỉ phân tử tham gia chuyển hóa đường thành rượu trong quá trình lên men. Enzyme là chất xúc tác sinh học đặc hiệu làm tăng tốc độ phản ứng, không bị biến đổi khi kết thúc phản ứng. Chất tham gia phản ứng do enzyme xúc tác được gọi là cơ chất.
– Enzyme có thể làm tăng tốc độ phản ứng lên hàng trăm nghìn đến hàng triệu tỉ lần so với phản ứng không có chất xúc tác. Khác với chất xúc tác vô cơ, enzyme có tính đặc hiệu với phân ứng và cơ chất Phân ứng do enzyme xúc tác thường diễn ra trong điều kiện phủ hợp với sự sống về nhiệt độ, độ pH, áp suất. Trong tế bảo, các phản ứng thưởng diễn ra theo chuỗi với nhiều loại enzyme cùng phối hợp tham gia. Đồng thời, các phản ứng được điều hòa nghiêm ngặt để tạo ra một lượng sản phẩm cần thiết mà không lãng phí cơ chất và không dư thừa sản phẩm.
| Enzyme là chất xúc tác sinh học đặc hiệu làm tăng tốc độ phản ứng, không bị biến đổi khi kết thúc phản ứng. |
b. Cấu trúc và cơ chế tác động của enzyme
– Hầu hết các enzyme có bản chất là protein Một số enzyme còn có thêm thành phần không phải là protein, được gọi là cofactor. Cofactor có thể là ion kim loại như Fe, Zn, Mg và hợp chất hữu cơ (còn gọi là coenzyme) có nguồn gốc từ vitamin nhu coenzyme NAD+, FAD.
– Phân tử enzyme có một vùng nhỏ có cấu trúc không gian tương ứng với cơ chất, liên kết đặc hiệu với cơ chất, làm biển đổi cơ chất được gọi là trung tâm hoạt động. Khi cơ chất liên kết vào, trung tâm hoạt động thay đổi hình dạng để khớp với cơ chất (mô hình “khớp cảm ứng”). Sự liên kết nảy thưởng bằng các liên kết yếu, tạm thời nhưng tạo điều kiện cho sự biến đổi cơ chất một cách nhanh chóng.
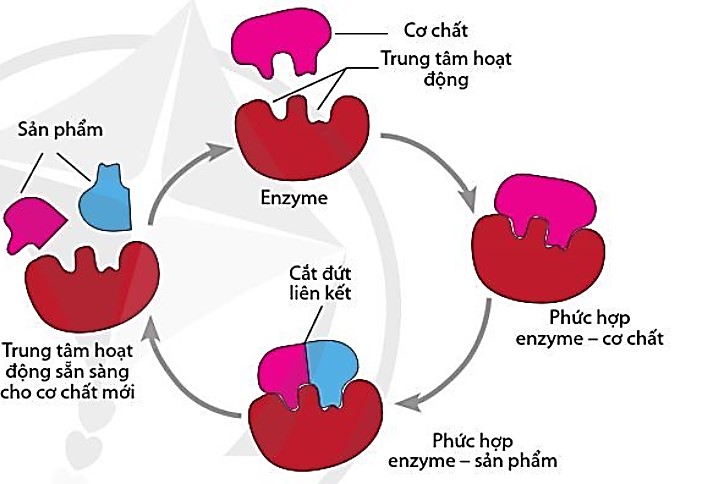
Hình 10.6. Ví dụ về cơ chế tác động của enzyme trong phản ứng phân giải
| Enzyme có cấu tạo chủ yếu là protein, ngoài ra có thể thêm cofactor (ion kim loại và hợp chất hữu cơ – coenzyme). |
c. Các yếu tố ảnh hưởng đến hoạt động xúc tác của enzyme
Hoạt động xúc tác của enzyme chịu tác động bởi nồng độ cơ chất, nồng độ enzyme và các yếu tố môi trường như nhiệt độ, độ pH, chất hoạt hoa, chất ức chế.
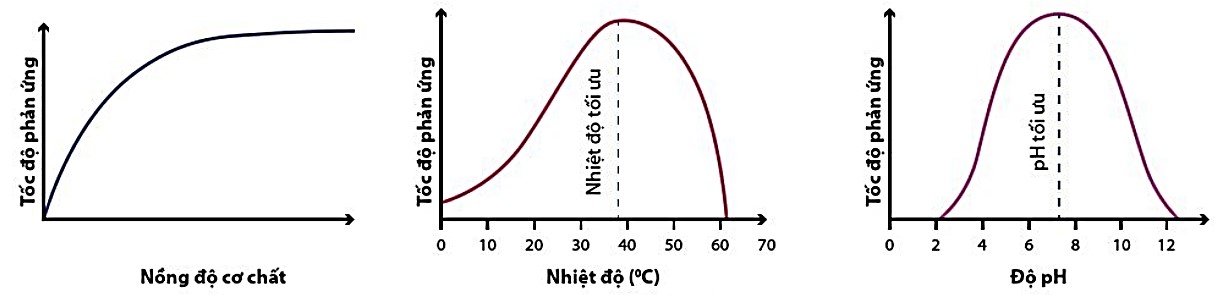
Hình 10.7. Đô thị minh hoạ ví dụ ảnh hưởng của một số yếu tố đến tốc độ phản ứng do enzyme xúc tác
– Khi nồng độ cơ chất tăng đến mức nhất định, tốc độ phản ứng. không tăng nữa (đạt cực đại) do toàn bộ enzyme đã liên kết với cơ chất. Trong điều kiện dư thừa cơ chất, khi tăng nồng độ enzyme thủ tốc độ phản ứng cũng tăng lên
– Mỗi enzyme thưởng hoạt động trong một dài nhiệt độ, pH nhất định. Ví dụ ở người, dải nhiệt độ hoạt động của enzyme là 25 – 40 °C, nhiệt độ tối ưu thưởng là 37 C. Nếu nhiệt độ tăng cao, enzyme sẽ bị thay đổi cấu trúc không gian và có thể dẫn đến mất hoạt tính hoàn toàn Enzyme thường hoạt động ở dài pH 6 – 8. Tuy nhiên, một số enzyme hoạt động trong môi trường acid (pepsin) hay kiểm (trypsin).
– Một số chất khi được bổ sung vào môi trường phản ứng ở nồng độ phù hợp làm tăng tốc độ phản ứng enzyme được gọi là chất hoạt hoá. Ví dụ NaCl là chất hoạt hoa amylase. Một số chất khác làm giảm tốc độ phản ứng enzyme hoặc dùng phản ứng enzyme được gọi là chất ức chế như một số ion kim loại nặng, một số loại thuốc.
| Khi xúc tác, enzyme liên kết với cơ chất tạo thành phức hợp enzyme – cơ chất và biến đổi cơ chất thành sản phẩm. Hoạt động xúc tác của enzyme chịu tác động bởi nhiều yếu tố như nồng độ cơ chất, nồng độ enzyme, nhiệt độ, độ pH, chất hoạt hoá và chất ức chế. |
1.3. Thực hành về enzyme
a. Ảnh hưởng của nhiệt độ đến hoạt tính của amylase
Chuẩn bị
– Hoa chất dung dịch tinh bột 0,5 %, dung dịch amylase, thuốc thử Lugol, nước cất.
– Dụng cụ ống nghiệm, cốc đựng nước đá (0 °C), cốc đựng nước ở khoảng 37 °C, cốc đụng nước sôi (100 °C)
Tiến hành
– Lấy ba ống nghiệm và đánh số các ống nghiệm.
– Cho 1 mL dung dịch amylase vào mỗi ống nghiệm
– Đặt ống 1 vào cốc đựng nước đá, ống 2 vào cốc đựng nước ở khoảng 37 °C, ổng 3 vào cốc dựng nước sôi và để yên trong 10 phút
– Thêm 1 mL dung dịch tỉnh bột vào mỗi ống nghiêm, lắc đều và đặt lại vào các cốc tương ứng. Để cố định trong 10 phút
– Thêm vào mỗi ống 1 giọt thuốc thử Lugol.
Quan sát sự thay đổi màu dung dịch trong các ống nghiêm
Báo cáo
– Bảo cáo kết quả thí nghiệm theo mẫu ở bài 6 và trả lời các câu hỏi sau
+ So sánh màu dung dịch trong các ống nghiệm. Ống nghiệm nào có sự thuỷ phân tinh bột dưới tác dụng của amylase? Giải thích
+ Nhiệt độ nào thích hợp cho hoạt động xúc tác của amylase trong thí nghiệm trên?
Thực hành: Phân tích ảnh hưởng của nhiệt độ lên hoạt tính enzyme catalase trong khoai tây
b. Ảnh hưởng của độ pH đến hoạt tính của amylase
Chuẩn bị
– Hoá chất dung dịch tinh bột 0,5 %, dung dịch amylase, dung dịch HCl 0,1N, dung dịch NaHCO3 1%, thuốc thủ Lugol, nước cất.
– Dụng cụ ống nghiêm
Tiến hành
– Lấy ba ống nghiệm và đánh số các ống nghiệm.
+ Cho 1 mL dung dịch amylase vào mỗi ống nghiệm.
+ Thêm 1 mL nước cất vào ống 1: 5 giọt dung dịch HCl 0,1N vào ống 2 và 5 giọt dung dịch NaHCO3 1% vào ống 3 và lắc đều
+ Thêm 1 mL dung dịch tinh bột vào mỗi ống, lắc đều và để cố
+ Thêm vào mỗi ống 1 giọt thuốc thử Lugol
+ Quan sát sự thay đổi màu dung dịch trong các ống nghiệm
Ảnh hưởng của pH đến hoạt tính của enzyme amylase
Báo cáo
Báo cáo kết quả thí nghiệm và trả lời các câu hỏi sau
– So sánh kết quả màu dung dịch trong các ống nghiệm. So sảnh hoạt tỉnh của amylase trong các ống nghiệm và giải thích. Độ pH tối ưu cho hoạt động xúc tác của amylase trong thí nghiệm trên là bao nhiêu?